首页 >> 综合 > 搜罗天下 >
科学家揭开TET2基因缺陷如何促进急性髓系白血病的发展
美国最大的癌症研究和治疗组织之一希望之城的科学家们已经确定,TET2 基因的低水平如何促进动物模型中急性髓性白血病的快速增长。细胞干细胞最近发表了这项研究。
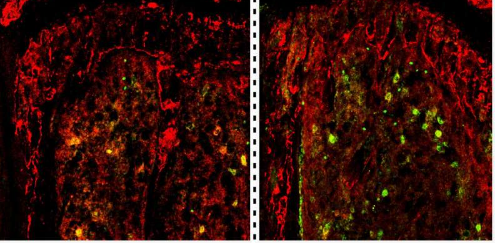
希望之城贝克曼研究所系统生物学西姆斯/曼家族基金会建陈博士领导的团队发现,TET2 缺乏会引发一系列生化变化,从而增强骨髓癌的能力传播。这些变化包括:
驱动恶性干细胞从血流移动到它们起源的骨髓区域。这种家庭微环境称为生态位,可以保护细胞的生存以及分裂和自我复制的能力。
增加一种名为 TSPAN13 的蛋白质的表达,该蛋白质向白血病干细胞发出信号返回骨髓生态位
导致 RNA 碱基胞嘧啶甲基化形式的形成,从而增强 TSPAN13 信使 RNA 的稳定性,从而导致 TSPAN13 蛋白表达增加
激活称为 TSPAN13/CXCR4 轴的信号通路,增加恶性干细胞返回(即归巢)骨髓微环境和自我复制,从而导致白血病的快速发展。
通过扩大对 TET2 影响急性髓系白血病发展的多种方式的理解,这一发现为治疗该疾病指明了新的潜在治疗靶点。
“这项研究为急性髓系白血病发展的细胞和分子机制提供了新的见解,”陈说。“我们的研究结果强调了在 TET2 突变或转录抑制患者中重新激活 TET2 信号传导的治疗潜力。同样令人兴奋的是,该策略可以应用于以 TET2 缺陷为特征的其他类型的癌症。”
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
分享:
相关阅读
最新文章
-
【梦到掉牙齿流血是什么预兆】梦境是人们日常生活中常见的现象,许多人都会做各种各样的梦。其中,“梦到掉牙...浏览全文>>
-
【梦到掉牙齿后流血预兆】梦境一直是人们关注的话题,尤其是那些带有强烈情绪或特殊象征意义的梦。其中,“梦...浏览全文>>
-
【梦到掉头发秃顶】梦境是人类潜意识的一种反映,常常带有象征意义。很多人在梦中会经历“掉头发”或“秃顶”...浏览全文>>
-
【梦到掉头发的预兆】梦境是人们潜意识的一种反映,而“梦到掉头发”是一个常见且令人不安的梦境。很多人在梦...浏览全文>>
-
【梦到掉水里好不好】梦境是人类潜意识的反映,不同的人对同一类梦境可能有不同的解读。而“梦到掉水里”是一...浏览全文>>
-
【梦到掉水里被救上来了】梦境是人类心理活动的一种表现形式,常常反映出内心的情绪、压力或潜意识中的想法。...浏览全文>>
-
【梦到掉上牙什么意思】梦境是人们日常生活中常见的一种心理现象,而“梦到掉牙齿”是一种非常普遍的梦境,尤...浏览全文>>
-
【梦到掉了一颗下牙】梦境是人类潜意识的一种表达方式,常常反映出我们内心的情绪、压力或未解决的困扰。其中...浏览全文>>
-
【梦到掉了两颗牙】梦境是人类潜意识的一种表达方式,常常反映内心的焦虑、压力或生活中的变化。其中,“梦到...浏览全文>>
-
【孟子说君子三乐是指那三乐】在《孟子·尽心上》中,孟子提出了“君子有三乐”,这是他对理想人格的一种阐述...浏览全文>>
大家爱看
频道推荐
